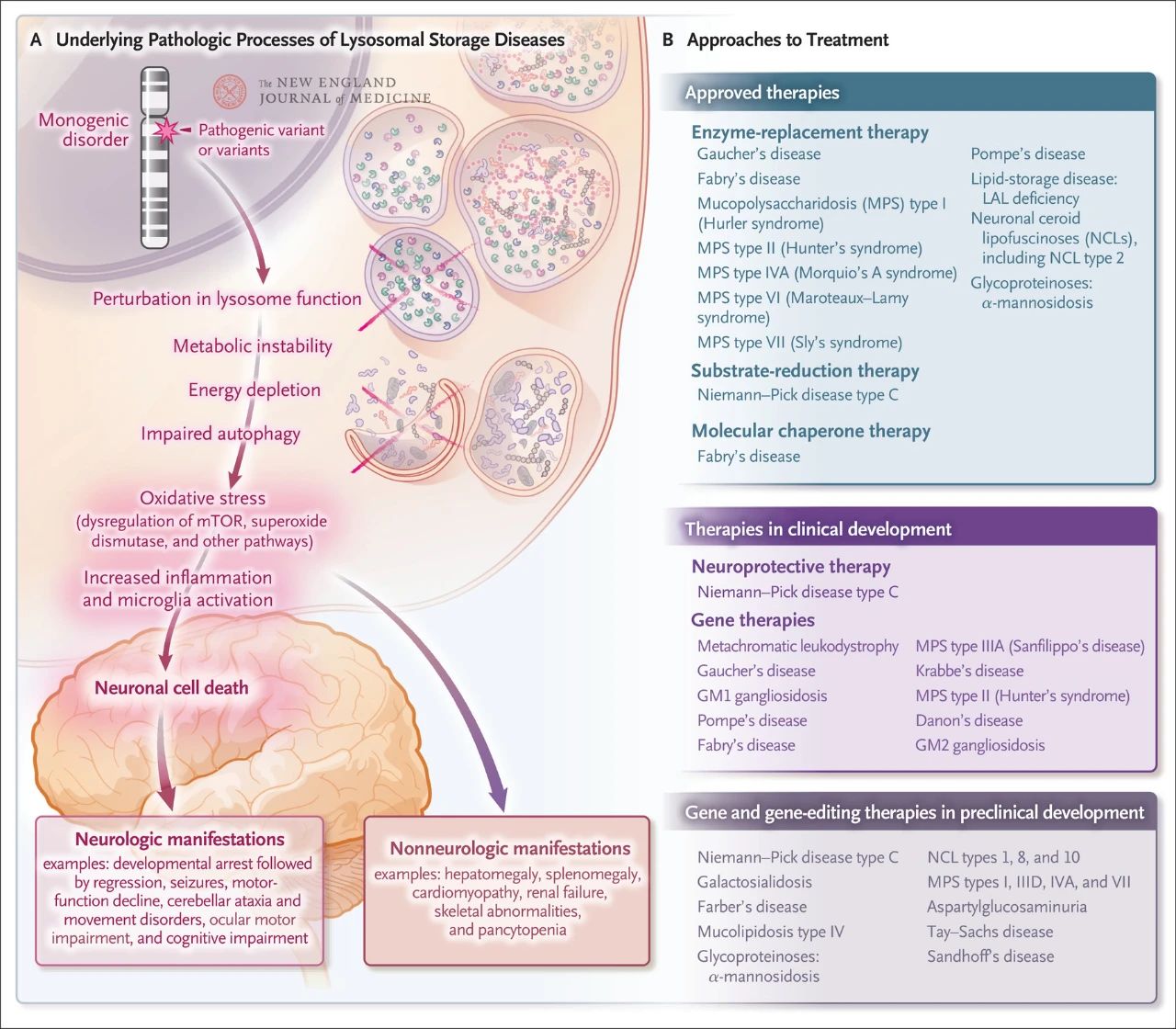
Nispeten nadir olsa da, lizozomal depolama hastalığının genel görülme sıklığı yaklaşık her 5.000 canlı doğumda 1'dir. Ayrıca, bilinen yaklaşık 70 lizozomal depolama bozukluğunun %70'i merkezi sinir sistemini etkiler. Bu tek gen bozuklukları, lizozomal işlev bozukluğuna neden olarak metabolik dengesizliğe, rapamisinin memeli hedef proteininin (normalde iltihabı engelleyen mTOR) düzensizliğine, bozulmuş otofajiye ve sinir hücresi ölümüne yol açar. Lizozomal depolama hastalığının altında yatan patolojik mekanizmaları hedef alan, enzim replasman tedavisi, substrat indirgeme tedavisi, moleküler şaperon tedavisi, gen tedavisi, gen düzenleme ve nöroprotektif tedavi dahil olmak üzere çeşitli tedaviler onaylanmış veya geliştirilme aşamasındadır.
Niemann-Pick hastalığı tip C, NPC1 (%95) veya NPC2 (%5) mutasyonlarından kaynaklanan lizozomal depo hücresel kolesterol taşıma bozukluğudur. Niemann-Pick hastalığının tip C'sinin semptomları arasında bebeklik döneminde hızlı ve ölümcül nörolojik gerileme yer alırken, geç juvenil, juvenil ve yetişkin başlangıçlı formları arasında splenomegali, supranükleer bakış felci ve serebellar ataksi, disartikülasyon ve ilerleyici demans bulunur.
Derginin bu sayısında, Bremova-Ertl ve arkadaşları çift kör, plasebo kontrollü, çapraz geçişli bir çalışmanın sonuçlarını bildirmektedir. Çalışmada, Niemann-Pick hastalığı tip C'yi tedavi etmek için potansiyel bir nöroprotektif ajan olan amino asit analoğu N-asetil-L-lösin (NALL) kullanılmıştır. 60 semptomatik ergen ve yetişkin hasta çalışmaya dahil edilmiş ve sonuçlar Ataksi Değerlendirme ve Derecelendirme Ölçeği'nin toplam puanında (birincil sonlanım noktası) önemli bir iyileşme göstermiştir.
NALL ve n-asetil-D-lösinin bir rasemiği olan N-asetil-DL-lösinin (Tanganil) klinik deneyleri büyük ölçüde deneyimle yönlendirilmiş gibi görünmektedir: etki mekanizması net bir şekilde açıklanmamıştır. N-asetil-DL-lösin, 1950'lerden beri akut vertigo tedavisi için onaylanmıştır; Hayvan modelleri, ilacın medial vestibüler nöronların aşırı polarizasyonunu ve depolarizasyonunu yeniden dengeleyerek etki ettiğini göstermektedir. Daha sonra Strupp ve arkadaşları, çeşitli etiyolojilere sahip dejeneratif serebellar ataksisi olan 13 hastada semptomlarda iyileşme gözlemledikleri kısa süreli bir çalışmanın sonuçlarını bildirmişlerdir; bu bulgular ilaca tekrar ilgiyi yeniden canlandırmıştır.
N-asetil-DL-lösinin sinir fonksiyonunu nasıl iyileştirdiği henüz net değil, ancak Niemann-Pick hastalığı tip C ve bir diğer nörodejeneratif lizozomal hastalık olan GM2 gangliozid depolama bozukluğu Varyant O (Sandhoff hastalığı) olmak üzere iki fare modelindeki bulgular, dikkatin NALL'a yönelmesine neden oldu. Özellikle, n-asetil-DL-lösin veya NALL (L-enantiyomerler) ile tedavi edilen Npc1-/- farelerin sağkalımı iyileşirken, n-asetil-D-lösin (D-enantiyomerler) ile tedavi edilen farelerin sağkalımı iyileşmedi; bu da NALL'ın ilacın aktif formu olduğunu düşündürmektedir. GM2 gangliozid depolama bozukluğu varyant O (Hexb-/-) ile ilgili benzer bir çalışmada, n-asetil-DL-lösin farelerde yaşam süresinin mütevazı ancak önemli bir şekilde uzamasıyla sonuçlanmıştır.
N-asetil-DL-lösinin etki mekanizmasını araştırmak için araştırmacılar, mutant hayvanların serebellar dokularındaki metabolitleri ölçerek lösinin metabolik yolunu incelediler. GM2 gangliozid depolama bozukluğunun bir varyant O modelinde, n-asetil-DL-lösin glikoz ve glutamat metabolizmasını normalleştirir, otofajiyi artırır ve süperoksit dismutaz (aktif bir oksijen temizleyicisi) seviyelerini yükseltir. Niemann-Pick hastalığının C modelinde, glikoz ve antioksidan metabolizmasında değişiklikler ve mitokondriyal enerji metabolizmasında iyileşmeler gözlemlendi. L-lösin güçlü bir mTOR aktivatörü olmasına rağmen, her iki fare modelinde de n-asetil-DL-lösin veya enantiyomerleri ile tedaviden sonra mTOR seviyesinde veya fosforilasyonunda bir değişiklik olmadı.
NALL'nin nöroprotektif etkisi, kortikal sıkışma kaynaklı beyin hasarı olan bir fare modelinde gözlemlenmiştir. Bu etkiler arasında nöroinflamatuar belirteçlerin düşürülmesi, kortikal hücre ölümünün azaltılması ve otofaji akışının iyileştirilmesi yer almaktadır. NALL tedavisinden sonra, yaralı farelerin motor ve bilişsel işlevleri geri kazanılmış ve lezyon boyutu küçülmüştür.
Merkezi sinir sisteminin inflamatuar yanıtı, çoğu nörodejeneratif lizozomal depo hastalığının ayırt edici özelliğidir. NALL tedavisiyle nöroinflamasyon azaltılabilirse, tüm nörodejeneratif lizozomal depo hastalıklarının olmasa da çoğunun klinik semptomları iyileştirilebilir. Bu çalışmanın da gösterdiği gibi, NALL'nin lizozomal depo hastalıkları için diğer tedavilerle sinerji yaratması beklenmektedir.
Birçok lizozomal depo bozukluğu serebellar ataksi ile de ilişkilidir. GM2 gangliozid depo bozukluğu (Tay-Sachs hastalığı ve Sandhoff hastalığı) olan çocuk ve yetişkinlerin yer aldığı uluslararası bir çalışmaya göre, NALL tedavisinden sonra ataksi azalmış ve ince motor koordinasyonu iyileşmiştir. Ancak, geniş çaplı, çok merkezli, çift kör, randomize, plasebo kontrollü bir çalışma, n-asetil-DL-lösinin karma (kalıtsal, kalıtsal olmayan ve açıklanamayan) serebellar ataksi hastalarında klinik olarak etkili olmadığını göstermiştir. Bu bulgu, etkinliğin yalnızca kalıtsal serebellar ataksi hastalarını içeren çalışmalarda ve ilişkili etki mekanizmalarının analiz edilmesinde görülebileceğini düşündürmektedir. Ayrıca, NALL travmatik beyin hasarına yol açabilen nöroinflamasyonu azalttığı için, travmatik beyin hasarının tedavisi için NALL denemeleri düşünülebilir.
Gönderi zamanı: 02 Mart 2024