Günümüzde, alkolsüz yağlı karaciğer hastalığı (NAFLD), Çin'de ve hatta dünyada kronik karaciğer hastalığının başlıca nedeni haline gelmiştir. Hastalık spektrumu basit hepatik steatohepatit, alkolsüz steatohepatit (NASH) ve ilişkili siroz ve karaciğer kanserini içerir. NASH, hepatositlerde aşırı yağ birikimi ve hepatik fibrozla birlikte veya tek başına indüklenen hücresel hasar ve inflamasyon ile karakterizedir. NASH hastalarında karaciğer fibrozunun şiddeti, kötü karaciğer prognozu (siroz ve komplikasyonları ve hepatoselüler karsinom), kardiyovasküler olaylar, karaciğer dışı maligniteler ve tüm nedenlere bağlı ölümle yakından ilişkilidir. NASH, hastaların yaşam kalitesini olumsuz etkileyebilir; ancak NASH'ı tedavi etmek için onaylanmış hiçbir ilaç veya tedavi yoktur.
New England Journal of Medicine (NEJM) dergisinde yayınlanan yeni bir çalışma (ENLIVEN), pegozaferminin biyopsiyle doğrulanmış sirotik olmayan NASH hastalarında hem karaciğer fibrozunu hem de karaciğer iltihabını iyileştirdiğini gösterdi.
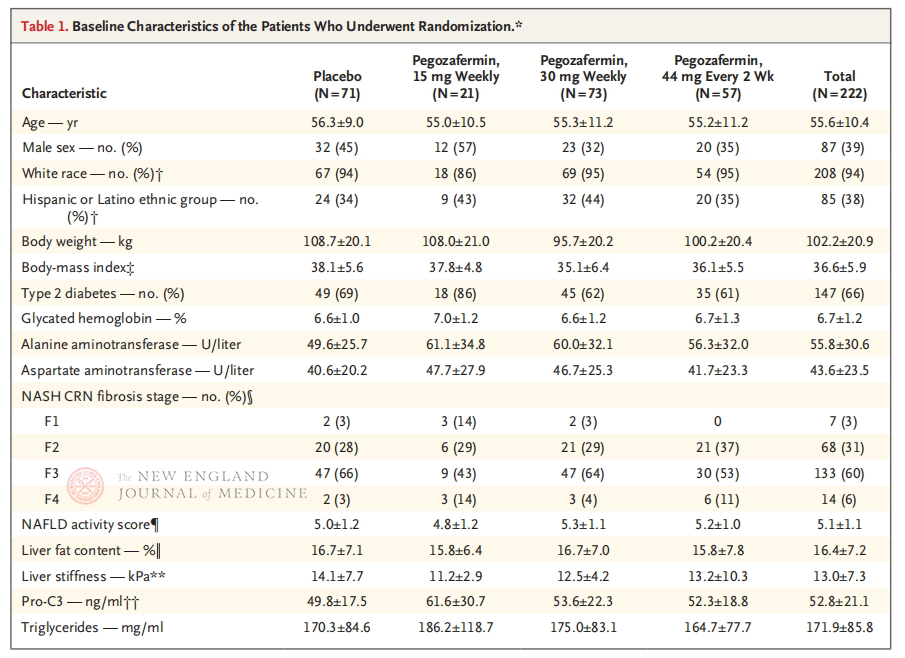
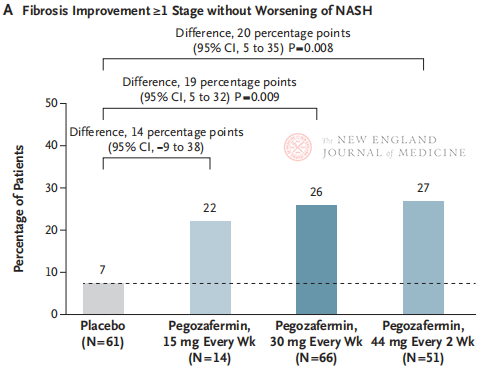
Kaliforniya Üniversitesi, San Diego Tıp Fakültesi'nde Profesör Rohit Loomba ve klinik ekibi tarafından yürütülen çok merkezli, randomize, çift kör, plasebo kontrollü Faz 2b klinik araştırmasına, 28 Eylül 2021 ile 15 Ağustos 2022 tarihleri arasında biyopsi ile doğrulanmış evre F2-3 NASH'li 222 hasta kaydedildi. Hastalar rastgele pegozafermin (subkutan enjeksiyon, haftada bir kez 15 mg veya 30 mg veya 2 haftada bir kez 44 mg) veya plaseboya (haftada bir veya 2 haftada bir) atandı. Birincil sonlanım noktaları arasında fibroziste ≥ evre 1 iyileşme ve NASH'de ilerleme olmaması yer aldı. NASH, fibrotik ilerleme olmadan iyileşti. Çalışmada ayrıca bir güvenlik değerlendirmesi de yapıldı.
24 haftalık tedaviden sonra, fibrozda ≥ evre 1 iyileşme ve NASH'de kötüleşme olmayan hastaların oranı ve NASH'de gerileme ve fibrozda kötüleşme olmayan hastaların oranı, üç Pegozafermin doz grubunda plasebo grubuna kıyasla anlamlı derecede daha yüksekti ve iki haftada bir 44 mg veya haftada bir 30 mg ile tedavi edilen hastalarda daha anlamlı farklar vardı. Güvenlik açısından pegozafermin plaseboya benzerdi. Pegozafermin tedavisiyle ilişkili en yaygın yan etkiler bulantı, ishal ve enjeksiyon bölgesinde eritemdi. Bu faz 2b çalışmasında, ön sonuçlar pegozafermin tedavisinin karaciğer fibrozunu iyileştirdiğini göstermektedir.
Bu çalışmada kullanılan pegozafermin, insan fibroblast büyüme faktörü 21'in (FGF21) uzun etkili glikolatlanmış bir analoğudur. FGF21, karaciğer tarafından salgılanan ve lipit ve glikoz metabolizmasının düzenlenmesinde rol oynayan endojen bir metabolik hormondur. Önceki çalışmalar, FGF21'in karaciğer insülin duyarlılığını artırarak, yağ asidi oksidasyonunu uyararak ve lipogenezi inhibe ederek NASH hastalarında terapötik etkilere sahip olduğunu göstermiştir. Ancak, doğal FGF21'in kısa yarı ömrü (yaklaşık 2 saat), NASH'in klinik tedavisinde kullanımını sınırlamaktadır. Pegozafermin, doğal FGF21'in yarı ömrünü uzatmak ve biyolojik aktivitesini optimize etmek için glikolatlanmış pegilasyon teknolojisini kullanır.
Bu Faz 2b klinik çalışmasındaki olumlu sonuçlara ek olarak, Nature Medicine'de (ENTRIGUE) yayınlanan bir başka yakın tarihli çalışma, pegozaferminin ayrıca şiddetli hipertrigliseridemisi olan hastalarda trigliseritleri, HDL olmayan kolesterolü, apolipoprotein B'yi ve hepatik steatozu önemli ölçüde azalttığını ve bunun NASH hastalarında kardiyovasküler olay riskini azaltmada olumlu bir etkiye sahip olabileceğini göstermiştir.
Bu çalışmalar, pegozaferminin endojen bir metabolik hormon olarak, özellikle NASH'in gelecekte metabolik olarak ilişkili yağlı karaciğer hastalığı olarak yeniden adlandırılabilmesi nedeniyle, NASH hastalarına çok sayıda metabolik fayda sağlayabileceğini göstermektedir. Bu sonuçlar, pegozafermin'i NASH tedavisi için çok önemli bir potansiyel ilaç haline getirmektedir. Aynı zamanda, bu olumlu çalışma sonuçları, pegozafermin'in faz 3 klinik çalışmalara katılımını destekleyecektir.
Her iki haftada bir 44 mg veya haftada bir 30 mg pegozafermin tedavisi, çalışmanın histolojik birincil sonlanım noktasına ulaşmış olsa da, bu çalışmadaki tedavi süresi yalnızca 24 haftaydı ve plasebo grubunda uyum oranı yalnızca %7 idi; bu oran, 48 hafta süren önceki klinik çalışmaların sonuçlarından önemli ölçüde düşüktü. Farklılıklar ve güvenlik aynı mı? NASH'in heterojenliği göz önüne alındığında, ilacın etkinliğini ve güvenliğini daha iyi değerlendirmek için gelecekte daha geniş hasta popülasyonlarını içeren ve tedavi süresini uzatan daha büyük, çok merkezli, uluslararası klinik çalışmalara ihtiyaç vardır.
Gönderim zamanı: 16 Eylül 2023